食管癌是一种常见的消化系统恶性肿瘤。该肿瘤的侵袭性强、易复发,约有50%的患者在初诊时即出现明显的转移。我国是食管癌的高发区,且我国的病例以食管鳞癌(ESCC)为主。因缺乏有效的分子靶点,经过治疗的ESCC患者其预后仍不理想,5年生存率< 30%。故急需加强该病的发病机理研究,以发现新的治疗靶点。代谢重编程研究为揭示ESCC的病理生物学特征提供了新视角。然而,驱动ESCC进展的关键代谢特征仍不明确。
2024年4月3日,我院陈文连研究员团队在国际权威期刊Cell Death & Differentiation(1区, IF 12.4)在线发表了题为Unveiling the methionine cycle: a key metabolic signature and NR4A2 as a methionine-responsive oncogene in esophageal squamous cell carcinoma的研究论文(论文链接:https://www.nature.com/articles/s41418-024-01285-7)。项目团队发现ESCC患者的肿瘤组织中有高度活跃的甲硫氨酸(Met)代谢,进一步发现ESCC细胞可大量摄取Met来合成甲基供体——S-腺苷甲硫氨酸(SAM),然后通过“METTL3-RNA m6A-IGF2BP2”轴,上调促癌基因NR4A2的mRNA稳定性和蛋白表达,最终促进ESCC进展。、

为阐明临床ESCC组织中的关键代谢活性,团队纳入了1个发现集队列和3个验证集队列,从代谢物和代谢酶表达水平上证实患者的肿瘤组织中存在异常活化的Met循环通路。进一步发现,Met循环通路可作为独立的临床参数来预测患者的不良预后。紧接着,团队证实ESCC细胞可大量摄取胞外Met来合成SAM,进而促进ESCC恶性生长。
为揭示Met促进ESCC进展的分子机制,团队开展了深入的研究。结果发现,ESCC细胞摄取Met合成SAM后,在writer酶METTL3介导下,上调核受体基因NR4A2 mRNA上的m6A甲基化;接着,reader蛋白IGF2BP2读取到该甲基化信息,从而促进NR4A2 mRNA的稳定性和蛋白表达,最后促进ESCC生长。功能研究发现,NR4A2是Met依赖的促癌基因,它对维持高Met条件下的ESCC细胞增殖是必需的。临床相关性分析发现,NR4A2在患者的肿瘤组织中显著高表达,并且瘤内NR4A2水平与患者生存时间呈负相关。因此,本研究新发现的Met响应基因NR4A2是ESCC治疗的新靶点。
最后,团队开展了药物筛选,发现一个非甾体消炎药——塞来昔布是NR4A2的有效抑制剂:该药物可结合并降解NR4A2蛋白,故该药物可显著抑制高Met饮食条件下的ESCC肿瘤生长。
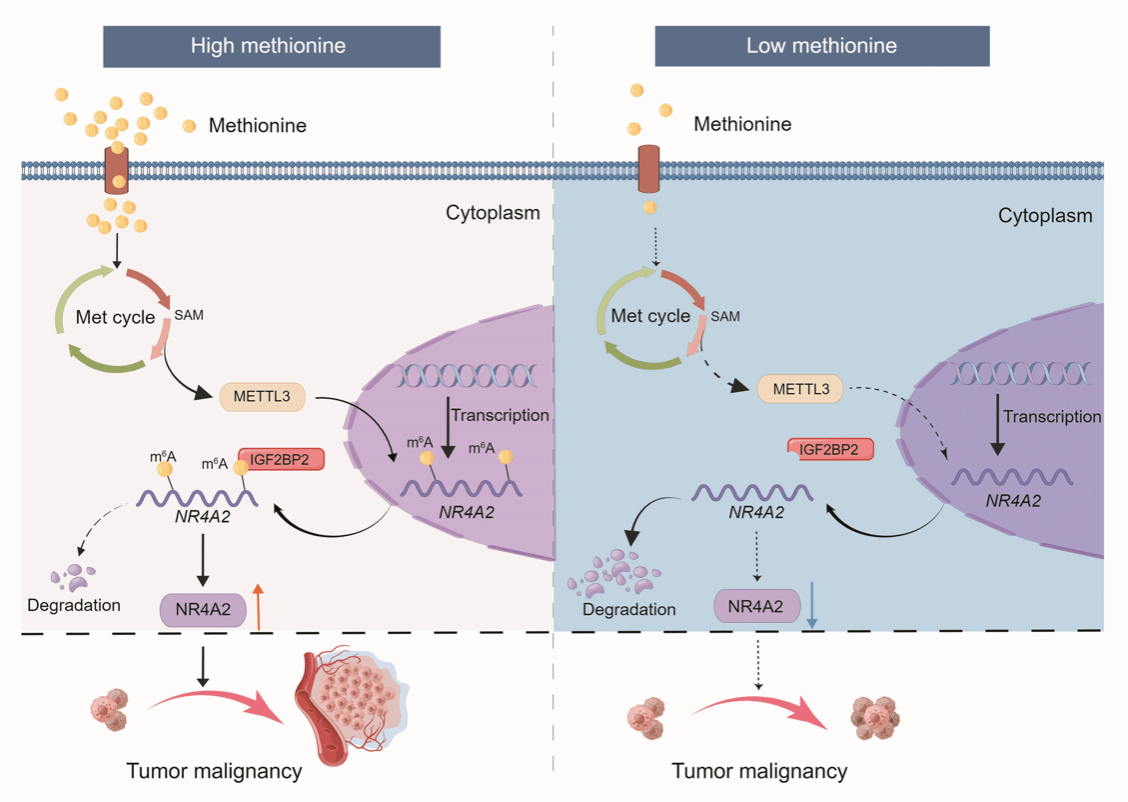
Met的促癌功能正日益受到重视。故Met限制性饮食已被用于抗肿瘤的临床前研究以及临床试验研究中。但是,Met作为一种人体必需氨基酸,对肌肉组织和神经系统非常重要。Met限制性饮食会造成体重减轻等副作用。因此,发现和鉴定受Met调控的下游关键促癌基因并用作新型抗肿瘤靶点,有助于克服Met限制性饮食带来的风险。本研究发现Met通过“SAM-METTL3-RNA m6A-IGF2BP2”这一新型调控轴来诱导ESCC细胞中的NR4A2表达,而NR4A2对Met的促癌功能不可或缺,故靶向干预NR4A2可作为替代Met限制性饮食的抗肿瘤新策略。
上海中医药大学附属龙华医院金星副研究员、南通市肿瘤医院胸外科刘雷医师、龙华医院肿瘤科刘丹医师为论文的共同第一作者,上海中医药大学附属龙华医院陈文连研究员为论文的通讯作者。本研究得到了国家重点研发计划项目、国家自然科学基金青年/面上项目、上海市炎癌转化病证生物学前沿研究基地等的支持。
(肿瘤研究所)